Division of Bioengineering, Incheon National University
119 Academy-ro, Yeonsu-gu, Incheon 22012, Republic of Korea

연세대학교 화공생명공학 박사
중앙대학교 화학공학 학사
| 기간 | 기관명 | 직위 및 직급 |
|---|---|---|
| 2019 – 현재 | 인천대학교 생명공학부 | 조교수 |
| 2014 - 2019 | Dept. of Materials, Imperial College London | Research Associate |

생명현상을 유지하기 위해 살아있는 세포는 매우 다양한 생물학적 기능과 화학반응을 수행하며, 이를 위해 세포 내에는 핵산(DNA, RNA), 단백질, 다당류와 같은 서열 조절이 가능한 생체고분자들이 존재합니다. 이들이 이루는 독특한 삼차원적 나노 구조와 분자간 상호작용으로 인해 세포는 다양하고 복잡한 신호전달 및 상호작용 네트워크를 형성하고 있습니다. 이러한 분자생물학적 기본 원리를 바탕으로 본 기능성 핵산나노재료 연구실(FuNNano Lab)에서는 1) 세포에서 발견되는 다양한 핵산 및 효소, 단백질의 구조와 생화학적 기능을 이해하고, 2) 이들을 빌딩 블록(building block)으로 사용하여 세포가 가진 분자적 기능을 뛰어넘는 다기능성 생체소재를 개발함으로써, 3) 바이오센서, 바이오이미징, 체외진단, 약물치료제, 백신전달체와 같은 생의학적 응용연구 뿐만 아니라 세포 및 생체분자의 상호작용을 연구하기 위한 생물학적 분자도구 개발을 위한 응용연구를 수행하고 있습니다.
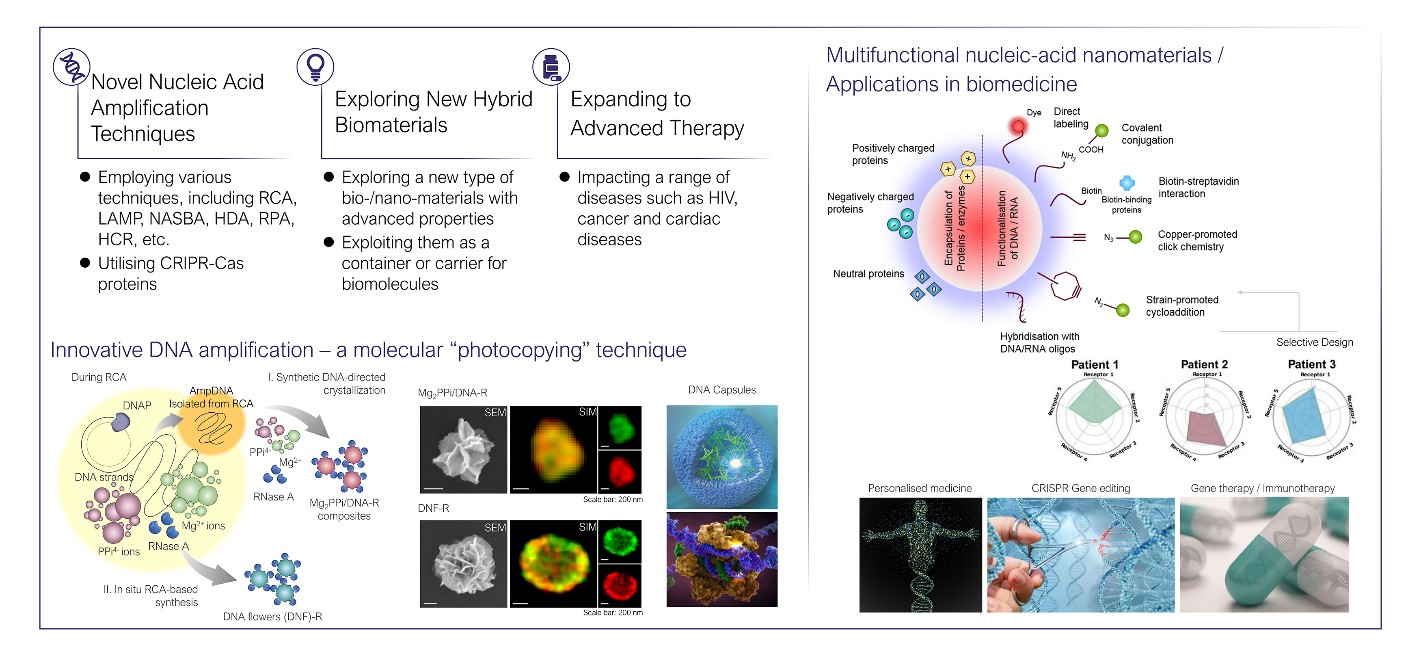
본 연구실에서는 생체고분자 중에서도 특히 핵산소재(DNA, RNA)를 이용하여 자가조립 물질(self-assemblies)를 합성하고, 이에 다양한 유무기 기능성 나노재료를 도입하여 응용 목적에 알맞게 설계된 다기능성 나노복합체(organic/inorganic hybrid nanocomposites)를 합성하는 연구를 수행하고 있습니다. 이렇게 합성된 핵산구조체는 생체물질 검출 및 모니터링을 위한 소재로서 생체 내 바이오마커를 고감도로 검출하고 분석할 수 있는 플랫폼으로 적용될 수 있습니다. 더 나아가 효과적인 질병 치료를 위해 약물을 비롯한 여러 형태의 치료용 유전자(siRNA, shRNA, miRNA, mRNA 등)를 생체 내 동시에 전달할 수 있는 전달체로도 응용하려는 연구를 수행하고 있습니다.
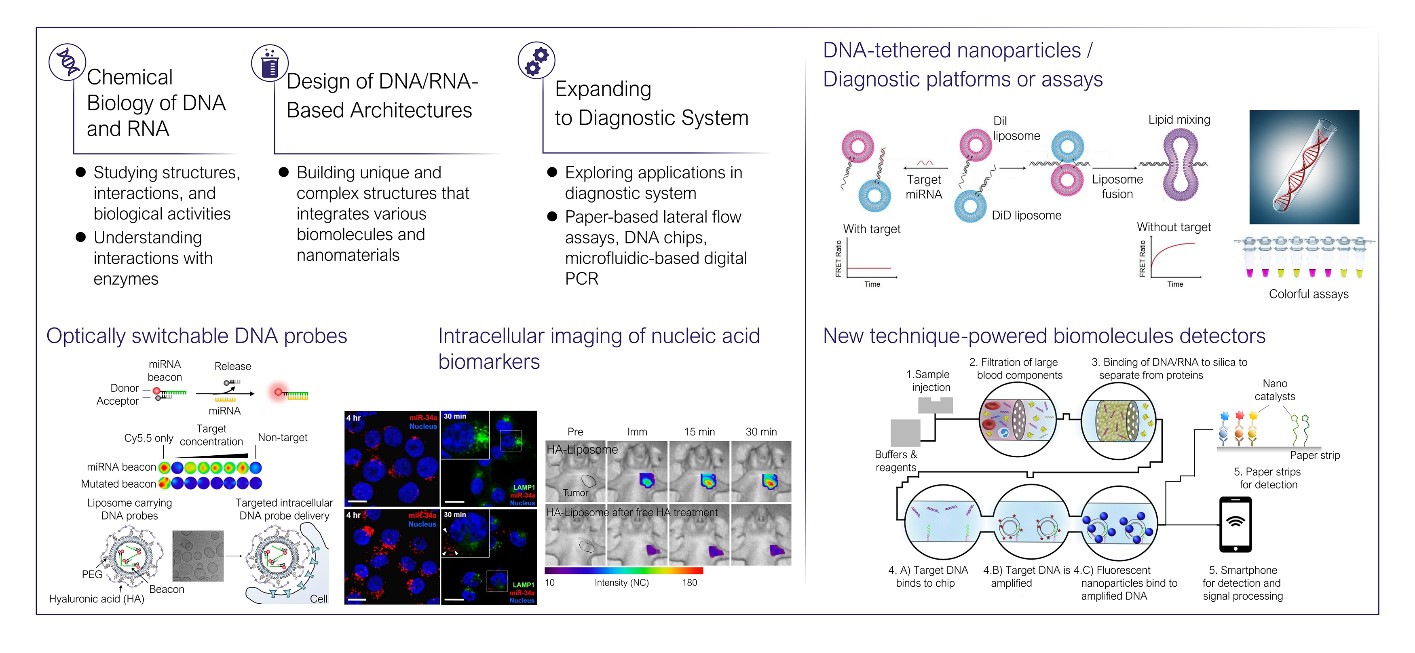
이 밖에도 세포막 수용체 인식 및 세포 내 신호전달 과정에서부터 조직 미세환경에 이르는 광범위한 생체시스템을 이해하고, 이를 바탕으로 세포내 소기관과 비슷한 크기와 성분으로 이뤄진 나노소재를 활용하여 약물의 안정적 전달과 선택적인 세포신호 기작을 유도할 수 있는 약물 전달체로 응용하기 위한 연구를 수행하고 있습니다. 이 연구에는 기능성 나노소재(리포좀, 폴리머 나노입자, 폴리머좀, 무기나노입자 등)를 합성하고, 나노입자의 표면 리간드(surface ligand)와 생체분자 혹은 생체시스템과의 계면(interface)에서 작용하는 물리화학적 상호작용을 다양한 분석기술을 이용하여 이해하는 것도 포함됩니다. 뿐만 아니라 향후 발생가능한 신변종 바이러스성 감염병에 대응하기 위한 백신 또는 면역증강제 전달 시스템에 대한 연구도 수행하고 있습니다.
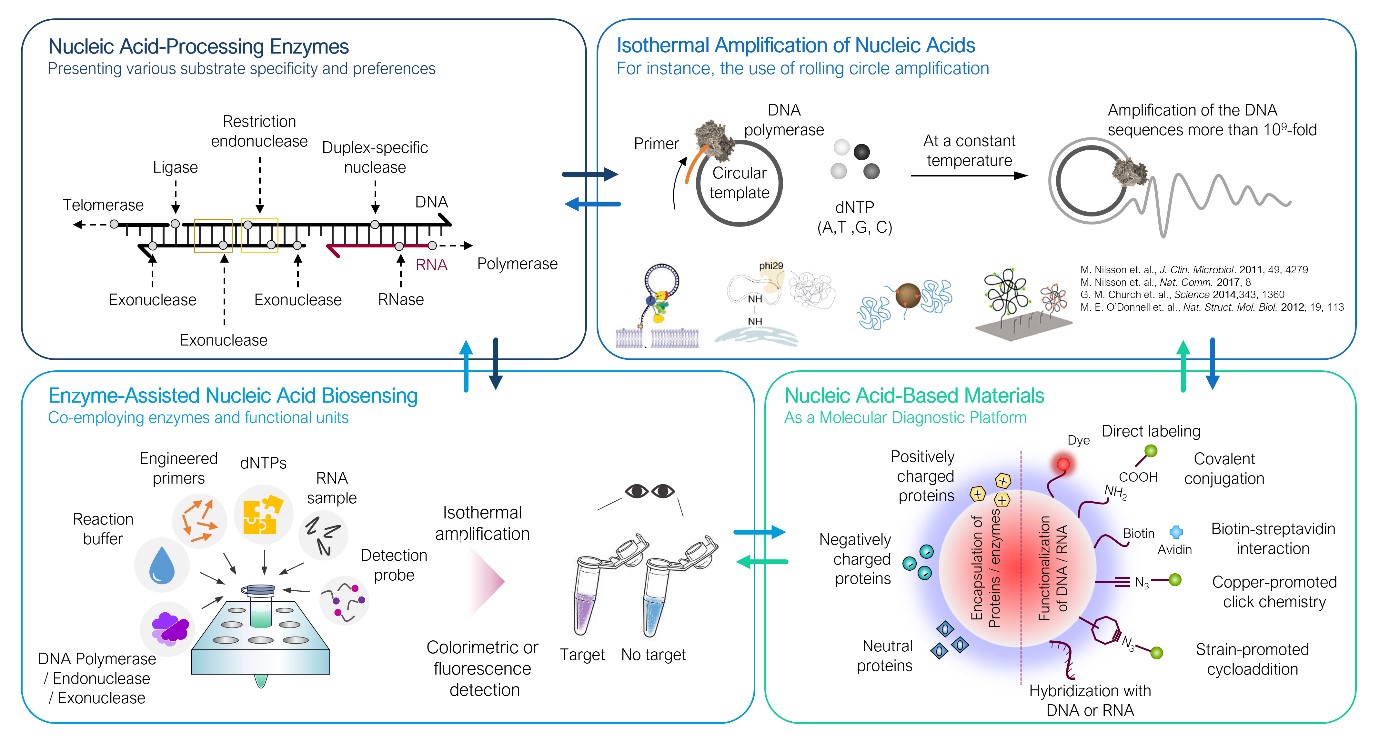
본 연구실은 핵산 처리효소(nucleic acid-processing enzymes)의 생화학적 기작과 생물학적 기능(중합, 절단, 분해, 접합, 결합 등)을 바탕으로 핵산효소의 반응을 선택적으로 유도할 수 있는 핵산 구조체 및 핵산 프로브를 설계하여 고성능 바이오센서, 분자스위치(molecular switch), 체외진단 기술에 적용하기 위한 연구를 수행하고 있습니다. 또한 특정 분자를 인식하여 이차원적인 구조 변이를 일으키는 압타머(aptamer)와 특정 분자에 대해 효소활성을 갖는 DNAzyme, RNAzyme을 활용하여 핵산효소와 함께 타겟물질에 대해 매우 특이적으로 연쇄적 신호증폭을 일으키는 고성능 등온 핵산증폭기술(isothermal amplification of nucleic acids)을 개발 중에 있습니다. 신호증폭 및 검출을 위한 형광나노입자를 개발하고 있으며, 이렇게 개발된 기술은 향후 바이오센서기술의 핵심기술로 활용되어 의료, 식품, 환경 및 군사 분야에 걸쳐 다양하게 적용될 수 있을 것으로 생각합니다.